AKEEGA™
Niraparib + abiraterone acetate
AKEEGA™は、PARP阻害薬(niraparib)と第2世代ホルモン剤(abiraterone acetate)を組み合わせた、最初で唯一の二重作用錠剤(すなわち固定用量配合(FDC)錠剤)です。病的変異または病的変異疑いのあるBRCA遺伝子変異転移性去勢抵抗性前立腺がん(mCRPC)患者への治療薬となり得ることから、より有効な治療薬を必要とするこれらの患者への対応促進に役立つと思われます。BRCA遺伝子変異が陽性のmCPRC疾患は悪性度が高い傾向にあり、mCRPC患者の約10~15%がBRCA遺伝子変異を有しています。Johnson & Johnson Innovative Medicineによる3番目の前立腺がん治療薬が、米国および欧州連合の両方で承認を取得したというマイルストーンの達成からは、患者の精密治療のための信頼できる予測バイオマーカーの重要性が浮き彫りにされています。2023年8月、Foundation Medicine Inc.は、niraparib + abiraterone acetateのコンパニオン診断薬として、FoundationOne®CDxの承認を米国FDAから取得しました。

Niraparib + abiraterone acetate 詳細情報
-
Johnson & Johnson Innovative Medicine
-
PARP阻害薬およびホルモン剤
-
BRCA遺伝子変異陽性mCRPC治療のために、プレドニゾンまたはプレドニゾロンとの併用により1日1回経口投与
-
また、HRR遺伝子変異を有する転移性ホルモン感受性前立腺がん(mHSPC)への使用も評価されています
-
約7万6千例の新規mCRPC症例(治療歴無)
-
約11万人が、2023年にG7市場でrmHSPCと新たに診断されています
なぜDrug to Watchなのか?
-
niraparib + abiraterone acetateの開発には、革新的でスマートなライフサイクル管理戦略が使用されています(特にabirateroneに後発医薬品が存在することが考慮されています)。非常に優れた有効性に加え、医師が肯定的な意見を持ち、処方を希望していることから、十分な市場競争力があります。固定用量配合(FDC)の単剤であるため、利便性の高い代替薬として使用できます。
-
米国FDAおよびEMAの承認は、mCRPC患者(相同組換え修復(HRR)関連遺伝子変異陽性または陰性)にniraparib + abiraterone acetateおよびプレドニゾンを投与し、転帰をプラセボ + abirateroneアビラテロン + プレドニゾン投与群と比較した大規模な第3相臨床試験(MAGNITUDE試験)の結果に基づくものです。
-
以下のような試験結果が得られています。
- BRCA1/2サブグループにおいて、画像診断による無増悪生存期間(rPFS)の中央値が19.5ヵ月(プラセボ + abiraterone群では10.9ヵ月)
- 全HRR+ コホートのrPFSの中央値が16.7ヵ月(プラセボ + abiraterone群では13.7ヵ月)
- ベネフィットリスクプロファイルに影響を及ぼす新たな安全性シグナルが存在しない、管理可能な安全性プロファイル
審査・承認状況
2022年4月
MAA提出:EMA
2023年2月
NDA提出:米国FDA
August 2023
sNDA/sBLA accepted: Mainland China NMPA
2023年4月
BRCA遺伝子変異陽性mCRPC患者へのプレドニゾンとの併用投与 承認:EMA
2023年8月
FDAが承認した検査により判定された病的変異または病的変異疑いのあるBRCA遺伝子変異陽性mCRPC患者 承認:米国FDA
上市年(実績・予測):
- 2023年 EU、米国
niraparib + abiraterone acetateは前立腺がん市場にどのような影響を与えるのか?
-
前立腺がんの全患者集団において、薬物治療の基本はホルモン剤による治療であり、新規薬剤(abiraterone、enzalutamideなど)を含むホルモン剤が今後も主要な薬剤クラスとしての位置を維持し、2032年までには前立腺がん市場全体の約50%を占めると予想されます。
-
しかし、PARP阻害薬および前立腺特異的膜抗原(PSMA)を標的とした放射性リガンドを含む新規標的薬が承認され、治療法の多様化が進んでいます。
-
後期開発段階のパイプラインには、さまざまな薬剤クラスおよび新規治療法(PARP阻害薬、キナーゼ阻害剤、PSMA標的放射性リガンド、血管新生阻害剤など)が存在します。
-
niraparib + abiraterone acetateは、市場を牽引する新規薬剤として、2032年には29億ドルの主要市場売上を獲得すると予想されます。niraparib + abiraterone acetateは投与期間が長く高価であるため、売上の75%はmHSPCの治療から得られると考えられます。
-
PARP阻害薬とホルモン剤の併用療法としては、他にも例えばAstraZeneca と MSDのLYNPARZA® + abirateroneなどが利用可能ですが、これらは「オープン」な併用療法であり、2種類の異なる錠剤をそれぞれ異なる投与スケジュールで投与する必要があります。C85
niraparib + abiraterone acetateはどのような治療上のギャップを埋めるのか?
mCRPCは、現在の標準治療では依然として治癒が不可能な疾患であり、BRCA陽性のmCRPC患者では疾患の悪性度が高く、転帰が不良で、生存期間が短い可能性が高くなります。 そのため、より有効な治療選択肢を提供できる新規MOA薬が必要とされています。PARP阻害薬はこのアンメットニーズの一部を満たすことができる可能性があり、予測バイオマーカーを使用する標的療法は、患者にとって最も有効なMOAの確実な提供に役立ちます。標的分子が特定されているこの患者サブセット用にすでに上市されているPARP阻害薬 + ホルモン剤の併用投与と比較して、niraparib + abiraterone acetateには投与スケジュールの利便性が高いという優位性があります(1日1回投与)。
ブロックバスターとなるために超えるべきハードルは?
niraparib + abiraterone acetateは、他のPARP阻害薬 + ホルモン剤の併用療法との激しい競合に直面する可能性が高いと考えられます。lynparzaとabiraterone acetateの併用には、BRCA陽性のmCRPC患者への第一選択治療として最初に上市された療法という利点があります。また、iynparzaは後方ラインの治療における単剤療法剤として早期から承認されているため、医師によりよく知られているという利点もあります。他のHRR変異を有する患者にも広く適用可能なTALZENNA®(Pfizer Inc)とXTANDI®(Pfizer Inc and Astellas Pharma Inc)の組み合わせも、競合製品となります。また、「オープン」な併用療法が提供する投与の柔軟性と費用削減をFDCの利便性よりも重視する腫瘍専門医も存在します。
$2.7B
95%
医薬品のタイムラインと開発成功確率
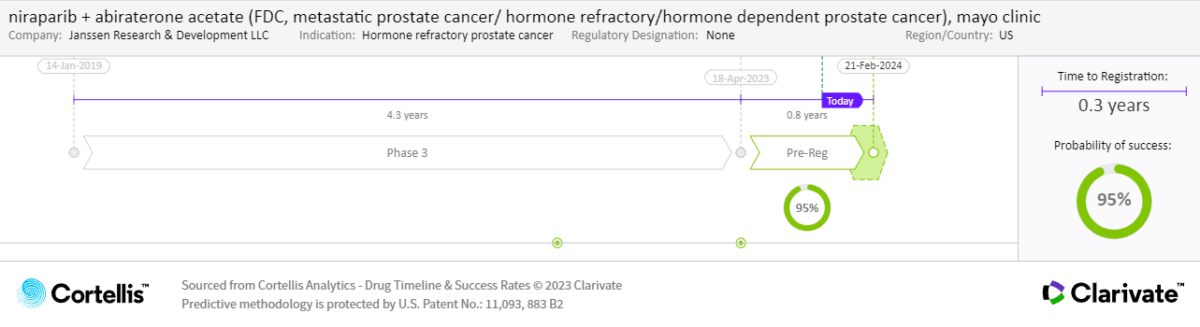
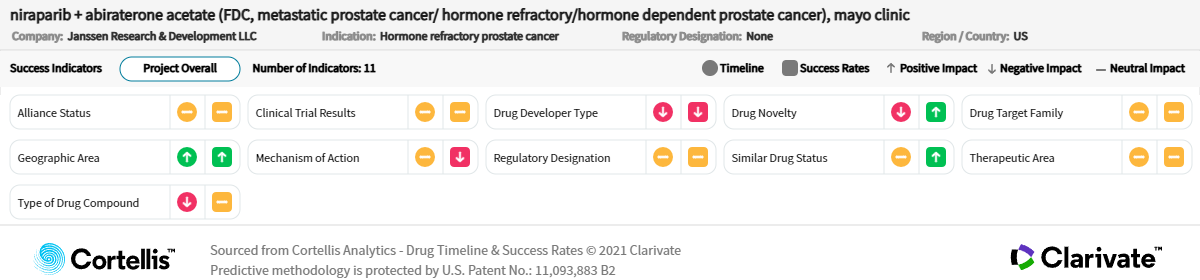
出典:Cortellis Competitive Intelligence、医薬品タイムライン と開発成功確率予測日 2022年12月15日