ALTUVIIIO™
Efanesoctocog alfa
BIVV001
efanesoctocog alfaは、週1回の静脈内投与による第VIII因子(FVIII)補充療法であり、現在使用可能な他のFVIII補充療法の投与頻度に伴う患者負担の軽減に役立ちます。モノクローナル抗体や遺伝子治療など、新規の治療に消極的な患者にとって、efanesoctocog alfaは魅力的なオプションとなる可能性が高いと考えられます。臨床医も、現在入手可能な臨床試験データから示されている達成可能FVIIIレベル、注射頻度および安全性プロファイルから、efanesoctocog alfaを肯定的に評価しています。
efanesoctocog alfaの開発および販売に関しては、サノフィ社が米国における権利を所有し、欧州およびその他の市場においてはSobi社が責任を負います。

Efanesoctocog alfa 詳細情報
-
サノフィ(Bioverativ Therapeutics Inc.)、Swedish Orphan Biovitrum AB
-
遺伝子組換えFVIII補充療法
-
成人および小児血友病A患者への、出血予防のための週1回の定期的静脈内投与、出血症状コントロールのためのオンデマンド治療および周術期の出血管理のための静脈内投与
-
約4万5千人が、2023年にG7市場で血友病Aであると診断されています
なぜDrug to Watchなのか?
-
より長時間にわたり循環血中に存在できるよう、efanesoctocog alfaには革新的なFc融合技術に加えてフォン・ヴィレブランド因子の一部とXTEN®ポリペプチドが追加されています。本剤は、現在のFVIII治療の半減期を制限していると考えられるフォン・ヴィレブランド因子による制限を受けないことが示されている唯一のFVIII製剤です。その結果、週1回のみの投与でのFVIII補充療法が可能となり、治療の負担が軽減されます。
-
データに基づいています。試験前にFVIII製剤による予防治療を受けていた患者には、定期的な予防治療としてefanesoctocog alfaが投与されました(A群)。試験前にFVIII製剤によるオンデマンド治療を受けていた患者には、26週間にわたりefanesoctocog alfaによるオンデマンド治療が行われた後、26週間にわたりefanesoctocog alfaによる定期的な予防治療が行われました(B群)。
-
efanesoctocog alfaの週1回予防投与により以下の試験結果が得られました。
- 年間出血率(ABR)の中央値は、A群が0、B群(オンデマンド治療)が21.1、B群(予防治療)が0でした。
- ABRの平均値は、A群が0.7、B群(オンデマンド治療)が21.4、B群(予防治療)が0.7でした。
- A群では、試験前の凝固因子製剤による予防治療との患者内比較で77%のABR減少が示されました
- >平均FVIII活性は1週間の大半にわたり40 IU/dL超が維持され、7日目で15 IU/dLでした
- ベースライン時に標的関節が認められたすべての被験者で、12ヵ月間のefanesoctocog alfaの予防的投与後にすべての標的関節で消失効果が見られました
- 患者により身体的健康および疼痛強度の改善が報告されています
- 本試験においてFVIII阻害の徴候は認められていません
-
FVIII製剤による治療歴のある重度血友病Aの小児患者(12歳未満)を対象に、52週間にわたって週1回のefanesoctocog alfa予防投与を行う第3相XTEND-Kids試験が実施され、以下の結果が得られました。
- ABRの中央値は0、平均値は0.89
- FVIII阻害の徴候は認められていません
-
以下の試験が現在進行中です。
- XTEND-ed:長期有効性および安全性を評価する延長試験
- FREEDOM試験:現在予防的治療を受けている12歳以上の重症血友病A患者を対象とした第3b相欧州試験
- 米国および日本における標準的治療を受けた血友病A患者に対するefanesoctocog alfaの実際の有効性、安全性および治療使用実態を調べる前向き、縦断的コホート研究
審査・承認状況
2017年8月
オーファンドラッグ指定:米国FDA
2019年6月
オーファンドラッグ指定:EMA
2021年2月
Fast track指定:米国FDA
2021年7月
画期的治療薬指定:中国本土
2022年6月
Breakthrough therapy指定:米国FDA
2023年2月
成人および小児血友病A患者 承認:米国FDA
2023年5月
製造販売承認申請(MAA)受理:EMA
2023年9月
成人および小児血友病A患者 承認:日本PMDA
上市年(実績・予測):
- 2023年: 日本、米国
- 2024年: EU
- 2028年: 中国本土
2032年以降に特許存続期間が満了しはじめると推定される
efanesoctocog alfaは血友病A市場にどのような影響を与えるのか?
-
血友病A治療市場には新薬が続々と登場しています。 C34
-
治療負担を軽減できる皮下投与療法が開発されていますが、現在のFVIII補充療法で良好な結果が得られている患者の多くは現在の治療を継続する可能性が高いと考えられます。これらの患者では、静脈アクセスが良好で、長年にわたる静脈内投与がすでに習慣化しており、出血もごくわずかな可能性があります。
-
新規の治療オプションにおいても、破綻出血は避けられない場合があります。このような出血に加えて、術後管理や外傷関連出血には引き続きFVIIIによる治療が必要です。
-
G7諸国における血友病A患者集団は、血友病患者の予想生存期間の中央値が人口の平均余命に近づいているため高齢化しています。治療可能な患者数が増加し、治療期間が全体的により長期化することに加えて、高齢の血友病A患者集団はFVIII持続注入などの止血介入が必要となる可能性のある大きな手術をより多く受けます。
-
凝固因子補充療法の用量は患者の体重に基づいて決定されるため、年齢に比例した体重増加に伴い薬剤消費量が増加し、最終的には薬剤の売り上げが増加します
efanesoctocog alfaはどのような治療上のギャップを埋めるのか?
血友病A治療の一番の目的は、出血、特に永続的な関節損傷につながる関節内出血を予防することです。さらに、もう一つの重要な目的として生活の質の改善があります。しかし、現在のFVIII補充療法は投与頻度および投与経路の点から患者負担が大きく、これが最適とはいえない治療継続率の一因となっています。efanesoctocog alfaは、週1回の静脈内投与によるFVIII補充療法を可能にした最初の薬剤であり、患者の利便性を改善し、治療負担を軽減させることで治療継続率を向上させることができます。
ブロックバスターとなるために超えるべきハードルは?
血友病の治療は、特に重度の出血傾向を有する患者においては高価な治療であるため、治療レジメンの価値の正確な定量化が臨床医と支払者の双方から求められます。より低コストの皮下投与治療オプションとして現在患者に利用可能なHEMLIBRA®(Genentech)の使用の増加が市場価値を抑制し続けています。また、新たに出現している遺伝子治療薬も、初期費用は高価となる可能性が高いと考えられますが、治癒的であるためFVIII補充療法など侵襲的な標準治療の必要性を低減させる可能性があります。
$1.77B
95%
医薬品のタイムラインと開発成功確率
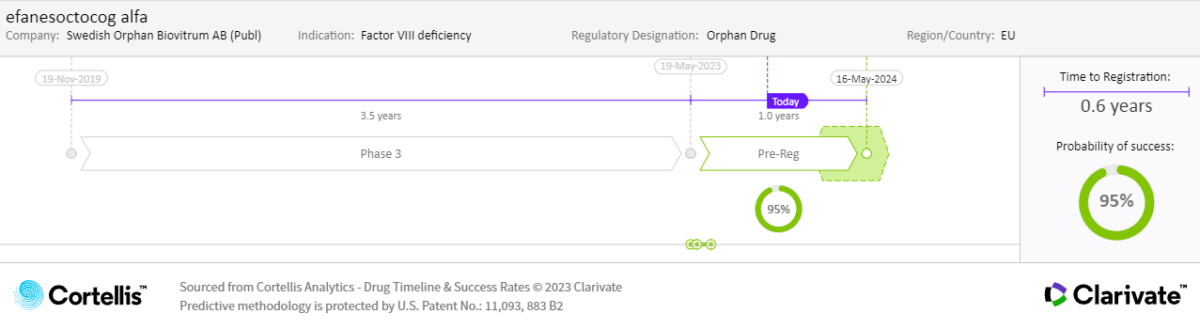
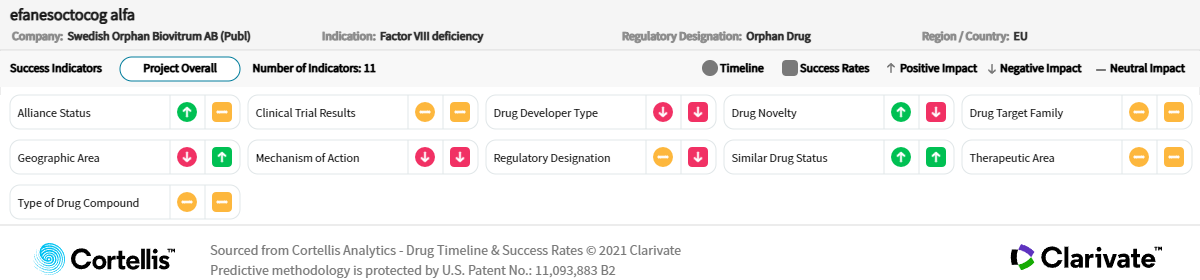
*出典:Cortellis Competitive Intelligence、医薬品タイムライン と開発成功確率予測日 2023年11月3日