AKEEGA™
Niraparib + abiraterone acetate
이 약은 PARP 억제제(niraparib)와 차세대 호르몬 요법(abiraterone acetate)을 결합한 최초이자 유일한 이중 작용(또는 고정용량복합제[fixed-dose combination, FDC]) 정제입니다. 유해하거나 유해한 것으로 의심이 되는 BRCA유전자 변이 양성 전이성 거세 저항성 전립성암(metastatic castration-resistant prostate cancer, mCRPC)에 대한 치료제로서의 능력은 보다 효과적인 치료를 필요로 하는 환자들의 요구를 충족하는데 도움이 될 것입니다. 전체 전이성 거세 저항성 전립선암 환자들 중 10%~15%가 BRCA유전자 변이를 나타내는데, 이 같은 BRCA유전자 양성 전이성 거세 저항성 전립선암 환자들은 공격적인 종양을 나타낼 가능성이 높습니다. 미국과 EU의 승인은Johnson & Johnson Innovative Medicine이 세번째 전립선 암치료제를 승인받으며 마일스톤에 도달했음을 의미합니다. 또한, 환자에 대한 정밀치료를 위한 신뢰할 수 있는 예측가능한 바이오마커가 중요함을 보여주기도 합니다. 2023년 8월, 미국 FDA는 Foundation Medicine Inc.의 FoundationOne®CDx 동반 진단으로 Niraparib + abiraterone acetate을 사용할 수 있도록 승인했습니다.

Niraparib + abiraterone acetate 소개
-
제조사:Johnson & Johnson Innovative Medicine
-
PARP 억제제 및 호르몬 요법
-
BRCA-양성 mCRPC 치료를 위해 프레드니손 또는 프레드니솔론과 병용하여 1일 1회 경구 투여.
-
HRR 유전자 변이가 있는 전이성 호르몬 민감성 전립선암(metastatic, hormone-sensitive prostate cancer, mHSPC)에 대해서도 평가 진행 중
-
7만 6천: 이전에 치료받지 않은 mCRPC신규 발생 증례
-
~11만건: 2023년 G7시장에서rmHSPC신규 발생 증례
블록버스터 신약 선정 이유
-
Niraparib + abiraterone acetate의 개발에는 창의적이고 스마트한 수명주기 관리 전략이 사용되었습니다(특히 abiraterone의 경우 제네릭이 출시되어 있다는 점을 고려할 때). 이는 매우 우수한 유효성 및 의사의 긍정적인 의견과 처방 욕구를 고려할 때 경쟁력이 있습니다. 단일 정제 내 FDC로서 이 약은 편리한 대안입니다.
-
미국 FDA와 EMA는 niraparib + abiraterone acetate + 프레드니손 병용요법을 투여받은 mCRPC 환자(상동 재조합 복구[homologous recombination repair, HRR] 관련 유전자 변이 유무에 관계없이)를 대상으로 위약+abiraterone+prednisone 병용요법을 투여받은 환자들의 결과와 비교한 대규모 제3상 임상시험(MAGNITUDE) 결과에 근거하여 이루어졌습니다.
-
그 결과는 다음과 같습니다:
- BRCA1/2 하위군의 방사선학적 무진행 생존(radiographic progression free survival, rPFS) 중앙값 16.6개월(vs 10.9개월 위약 + abiraterone acetate)
- 전체 HRR+ 코호트에서 rPFS 중앙값 16.5개월(vs 13.7개월위약 + abiraterone acetate)
- 관리 가능한 안전성 프로파일, 유익성-위해성 프로파일에 영향을 미치는 새로운 안전성 실마리정보 없음
심사 및 승인 상태
2022년 4월
MAA신청: EMA
2023년 2월
NDA신청: 미국 FDA
2023년 4월
Prednisone과 병용하여 BRCA-양성 mCRPC 환자 대상 승인: EMA
2023년 8월
FDA 승인 검사로 검출된 유해한 또는 유해한 것으로 의심되는 BRCA-양성 mCRPC 환자 대상 승인: 미국 FDA
실제 및 예상 출시:
- 2023년: EU, 미국
Niraparib + abiraterone acetate가 전립선암 치료제 시장에 미칠 영향은?
-
호르몬 요법은 모든 환자 집단의 약물 치료의 초석입니다. 호르몬 요법은 2032년까지 전체 전립선암 시장의 50%를 차지할 것으로 예상되는 새로운 호르몬 요법(예, abiraterone, enzalutamide)을 포함해 여전히 지배적인 약물 계열로 남아있을 것입니다.
-
그러나 PARP 억제제 및 전립선 특이적 막 항원(prostate-specific membrane antigen, PSMA) 표적 방사성리간드와 같은 혁신적인 치료제 승인으로 인해 치료법이 점점 더 다양화되고 있습니다.
-
후기 단계 파이프라인은 광범위한 약물 계열과 새로운 요법(예: PARP 억제제, 키나아제 억제제, PSMA 표적 방사성리간드, 혈관신생 억제제)에 걸쳐 있습니다.
-
Niraparib + abiraterone acetate는 2031년에 28억 달러의 주요 시장 매출을 달성하며 매출을 주도하는 신흥 약제가 될 것입니다. 긴 치료 기간과 niraparib + abiraterone acetate의 높은 가격으로 인해 이러한 매출의 75%는 호르몬 반응성 전이성 전립선암(mHSPC) 환자 치료영역에서 발생할 것입니다.
-
다른 PARP 억제제+호르몬 요법 병용요법(예: AstraZeneca와 MSD의 Lynparza + abiraterone)도 있지만, 이는 ‘개방형’ 병용(즉, 두 가지 약물을 다른 투여 일정에 따라 별도의 정제로 투여하는 것)입니다.
Niraparib + abiraterone acetate는 어떤 치료 공백을 메울 수 있는가?
mCRPC는 현재 표준 치료 요법으로는 여전히 치명적인 질병이며, BRCA 양성 mCRPC 환자는 질병이 공격적으로 진행되고 예후가 좋지 않으며 생존 기간이 짧을 가능성이 더 높습니다. 보다 효과적인 치료옵션을 제공하기 위해서는 새로운 작용기전을 가진 약물이 필요합니다. PARP억제제는 이러한 미충족된 요구를 부분적으로 충족시킬 수 있는 잠재력을 가지고 있으며, 예측가능한 바이오마커를 활용하는 표적치료법은 환자가 가장 효과적인 작용기전과 일치되도록 보장하는 것을 도울 것입니다. 이전에 시장에 나온 PARP 및 호르몬 약물 치료제 병용요법은 특정 유전자 변이 또는 특성에 기반하여 정의된 환자 하위그룹 치료를 위한 것으로 기존의 치료법에 비해Niraparib + abiraterone acetate는 보다 편리한 투약 일정(일일 투여량)을 제공합니다.
Niraparib + abiraterone acetate가 블록버스터 신약이 되기 위해 극복해야 하는 문제는?
Niraparib + abiraterone acetate는 다른 PARP억제제 및 호르몬 치료제 병용요법과 치열하게 경쟁하게 될 것입니다. Lynparza는abiraterone acetate 와 병용해 BRCA유전자 변이 양성 전이성 거세 저항성 전립성암의 1차 치료라인으로 시장에 최초로 출시된 이점을 가지고 있습니다. Lynparza는 또한 후기 라인에서 단독요법 치료제로 보다 일찍 출시되었기 때문에 의사들의 친숙도가 높습니다. 또 다른 경쟁제품인TALZENNA®(Pfizer Inc)는 XTANDI®(Pfizer Inc및Astellas Pharma Inc)와 병용하여 다른 HRR 돌연변이가 있는 환자에게도 확장되는 광범위한 용도를 가지고 있습니다. 또한, 일부 종양학자들은 고정형 조합보다 “개방형 조합”에 의해 제공되는 투여에 있어서의 유연성과 비용 절감을 선호할 수 있습니다.
$27억
95%
Drug Timeline & Success Rates
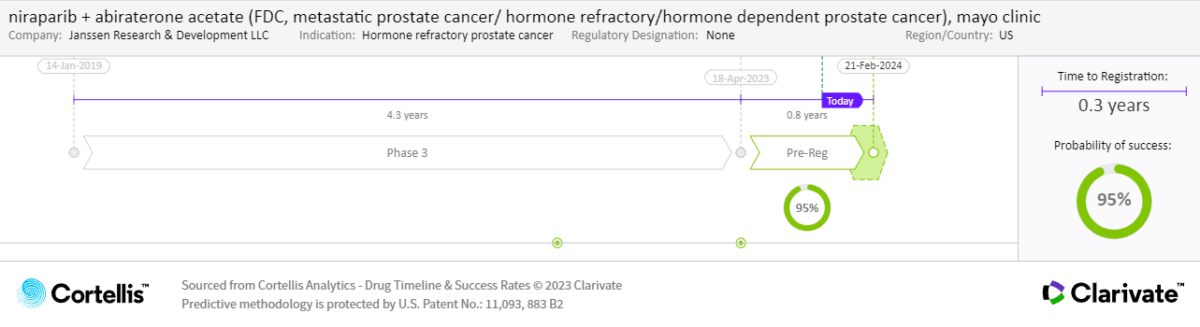
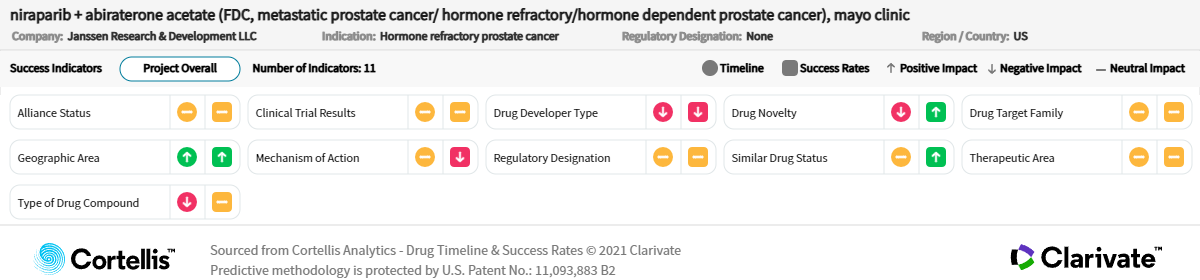
출처: Cortellis Competitive Intelligence, Drug Timeline & Success Rates Prediction, 2023년 11월 3일 기준