exa-cel
Exagamglogene autotemcel
CASGEVY™
鎌状赤血球症(SCD)およびβサラセミアに対する初の疾患修飾薬となるexagamglogene autotemcel(exa-cel)およびlovotibeglogene autotemcelが大きな注目を集めています。これらの疾患は人生を変えてしまうほどの消耗性疾患ですが、現在利用可能な対症療法や治癒的治療が限られているため、これらの治療薬の開発は極めて大きな成果となります。exagamglogene autotemcelは世界で初めて承認されたCRISPR/Cas9遺伝子編集治療薬としても注目されており、この承認が土台となり今後他の領域でもこの種の治療薬の承認が進む可能性があります。

Exagamglogene autotemcel詳細情報
-
CRISPR Therapeutics and Vertex Pharmaceuticals Inc
-
体外CRISPR/Cas9 遺伝子編集治療
-
重度のSCDおよび輸血依存性βサラセミアの治療のために、骨髄破壊的な化学療法後に自己造血幹細胞移植(HSCT)として静脈内注入する
なぜDrug to Watchなのか?
-
遺伝性血液疾患であるSCDおよびβサラセミアは、重度の疼痛、臓器損傷および短寿命の原因となります。これらの治療剤は、1回のみの投与でSCDおよび輸血依存性βサラセミアの根底にある原因を治療し、患者の輸血の必要性を軽減させ、血管閉塞発危機(VOC)の発生を抑えることで、生活の質および身体能力を有意に改善させることを目的としています。この分野における遺伝子治療への期待は、この治療の潜在的な治療効果のみならず、現在の他の治療法の有効性、利便性および副作用に関する懸念にも基づくものです。 SCD治療の最近の評価において, Institute for Clinical and Economic Review(ICER)は、いずれの治療剤も、長期持続性および有害性はまだ明確ではないものの、疾患の重症度および治療成功率を考慮に入れると、標準治療よりも大きな健康上の利点が得られる可能性があるという考えを示しています。
-
exagamglogene autotemcelは、ヒトの疾患の根本的な遺伝的原因を標的とした新しい治療法を発見および開発するために、CRISPR/Cas9に焦点を当てて2015年に開始されたVertexとCRISPR Therapeuticsとの共同研究プログラムから生み出された最初の治療剤です。ICERは、exagamglogene autotemcelを標準治療と比較して「同等またはそれ以上」と評価しています。
-
MHRA CMAおよび他の規制当局への承認申請は、以下に示す2つのピボタル第1/2/3相試験のデータに基づいて行われました。
-
CLIMB-111:
- VOCの再発を特徴とする12~35歳の輸血依存性βサラセミア患者
- 88.9%が12ヵ月以上連続して輸血することなく過ごせました
- 輸血を必要としない期間の平均値は20.5ヵ月(最長40.7ヵ月)
- 平均ヘモグロビン量は9 g/dL
- 全ヘモグロビンの平均値が8.9 g/dLから16.9 g/dLに増加
- 胎児ヘモグロビン(HbF)の割合の平均値が67.4%から99.6%に増加
-
CLIMB-121:
- VOCの再発を特徴とする12~35歳のSCD患者
- 94.1%で12ヵ月以上連続してVOCが発生しませんでした
- VOCが発生しない期間の平均値は18.7ヵ月(最長36.5ヵ月)
- 100%が12ヵ月以上連続してVOC関連の入院を必要としませんでした
- 全ヘモグロビンの平均値が11 g/dLから15.9 g/dLに増加
- 胎児ヘモグロビン(HbF)の割合の平均値が39.6%から49.6%に増加
- EuroQolのVisual Analog Scale(EQ VAS)およびFunctional Assessment of Cancer Therapy-General(FACT-G)とFunctional Assessment of Cancer Therapy-Bone Marrow Transplant(FACT-BMT)のスコアのベースライン平均変化が、6ヵ月時点において臨床的に重要な最小差(MCID)に達しており、18ヵ月間の追跡調査期間を通じて維持されていました
いずれの試験においても、安全性プロファイルは、ブスルファンおよびHSCTによる骨髄破壊的前処置とほぼ同一であり、潜在的なオフターゲット作用は検出されませんでした さらに、以下の第3相試験が継続中です。
-
CLIMB-141: 試験:2~11歳の、VOCの再発を特徴とする輸血依存性βサラセミア患者
-
CLIMB-151試験:2~11歳の、VOCの再発を特徴とするSCD患者
-
CLIMB-161試験:初期承認および発売後の製造施設の拡張をサポートするための試験;VOCの再発を特徴とする輸血依存性βサラセミアまたはSCDを有する12~35歳の患者
CLIMB-111試験、CLIMB-121試験、CLIMB-151試験およびCLIMB-161試験被験者は、最長15年間の長期的な安全性および有効性評価のためにCLIMB-131試験に継続して参加することが求められます。
審査・承認状況
2019年1月
SCD患者 Fast track指定:米国FDA
2019年4月
輸血依存性βサラセミア患者 Fast track指定:米国FDA
2019年10月
輸血依存性βサラセミア患者 オーファンドラッグ:EMA
2020年1月
SCD患者 オーファンドラッグ:EMA
2020年4月
輸血依存性βサラセミア患者 オーファンドラッグ:米国FDA
2020年5月
SCD患者 オーファンドラッグ:米国FDA SCDまたは輸血依存性βサラセミア患者 再生医療先端治療(RMAT)指定:米国FDA
2020年9月
SCD患者 PRIME指定:EMA
2021年4月
輸血依存性βサラセミア患者 PRIME指定:EMA
2023年1月
SCD患者 MAAバリデーション済み:EMAおよび英国MHRA
2023年4月
SCD患者 BLA承認:米国FDA 輸血依存性βサラセミア患者 BLA承認申請:米国FDA
2023年8月
SCD患者 Priority review指定:米国FDA
2023年10月
再発性の血管閉塞危機(VOC)を有する12歳以上の輸血依存性βサラセミアまたはSCD患者で、ヒト白血球抗原一致造血幹細胞提供者が存在しない患者 CMA:英国MHRA
2023年12月8日
For patients ≥12 years old with SCD with recurrent VOCs Approved: U.S. FDA
2024年3月30日
輸血依存性βサラセミア患者 PDUFA date
SCDまたは輸血依存性βサラセミア患者
上市年(実績・予測):
- 2023年: 英国
- 2024年: EU、米国
2033年以降に特許存続期間が満了しはじめると推定される
exagamglogene autotemceとlovotibeglogene autotemcelはSCDおよびβサラセミアの市場にどのような影響を及ぼすか?
-
SCDおよびβサラセミアは治療が困難な疾患であるため、上市される新治療薬は少なく、2017年に承認されたENDARI(Emmaus Medical Inc.)は20年ぶりに登場した新治療薬でした。
- これらの疾患に対する初の治癒的治療薬であるexagamglogene autotemcelおよびlovotibeglogene autotemcelにより、治癒的治療薬の今後の開発への道が開かれる可能性があります。
- ただし、いずれの治療法も費用が高く、適応患者集団が限られているため、利用が制限される可能性があります。
- しかし、ICERでは、これらの治療薬により、両疾患に関連するヘルスケアコストを低減させることが可能であり、VOCを回避できることで、標準的な治療と比較して治療費を最大11,600ドル(1回のVOCあたり)低減できると予測しています。
これらの治療薬はどのような治療上のギャップを埋めるのか?
SCDおよび輸血依存性βサラセミアには、症状管理に有用ないくつかの治療薬が存在しますが、多くの患者は生涯にわたり毎月の輸血を必要とします。このため、頻繁に通院して、極度の疼痛危機の発生を防ぎ、臓器損傷を最小限に抑え、生活の質を向上させて日常生活を完遂できるようにしています。しかし、定期的な輸血は、鉄過剰により心臓や肝臓疾患などの重篤な合併症を引き起こす可能性があり、これを回避するために長期的なキレート療法が必要となります。現在、鎮痛薬以外の治療選択肢はほとんど存在しません。HSCTはSCDの根治的治療となり得ますが、多くの患者には適合する血縁ドナーが存在せず、移植片対宿主病(GVHD)は深刻なリスクであり、HSCTのリスクは年齢とともに増大します。したがって、疾患修飾薬および根治療薬に対する重大なアンメットニーズが依然として存在します。
ブロックバスターとなるために超えるべきハードルは?
SCDおよび輸血依存性βサラセミアにおいては多部門にまたがるケアが必要ですが、医師への教育や協調的なケアの不足がしばしばその障害となります。ICERは、組織的な人種差別、貧困および複数の診療科でのケアを必要とする慢性疾患患者のために協調的なカバレッジを提供できるようにはデザインされていない保険システムもケアへのアクセスの障害因子となり得ると報告しています。さらに、臨床試験以外で報告された有効性および安全性の結果を一般化することが可能かどうかは不明です。
exagamglogene autotemcelは、まず重症患者に限定して使用される可能性が高く、すぐにインフラを整備できる機関が限られる可能性があり、適応患者の多くにとっては費用が高過ぎる可能性があります。この治療では治療前に骨髄破壊的な化学療法を行うことが必要ですが、卵子/精子凍結保存は保険適用が制限されることが多く、これによっても本治療薬の使用が制限される可能性があるという懸念も存在します。
Lovotibeglogene autotemcelは、生涯にわたるモニタリングを必要とする血液学的悪性腫瘍に対するブラックボックス警告や、発売当初はexagamglogene autotemcelよりも高いと見積もられている高額な費用が、治療への取り込みを妨げる可能性がある。また、治療へのアクセスは、複雑な遺伝子治療を実施するための専門訓練を受けた認定治療センター(QTC)に限られている。
$1.32B
95%
医薬品のタイムラインと開発成功確率
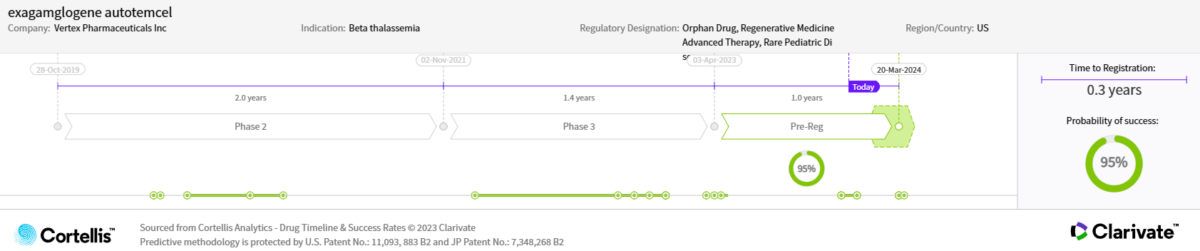
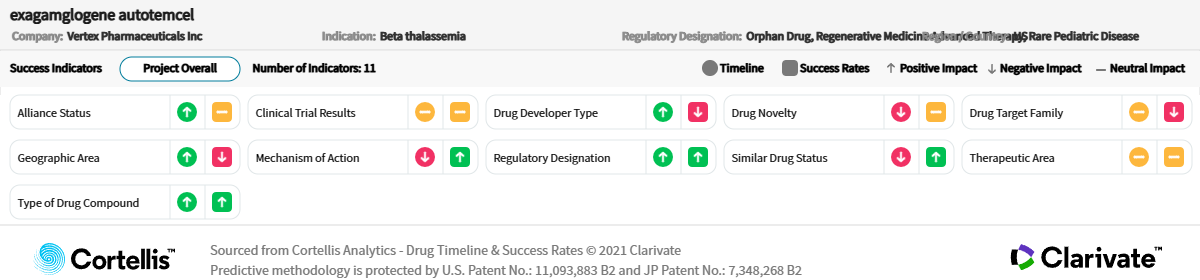
出典:Cortellis Competitive Intelligence、医薬品タイムライン と開発成功確率予測日 2023年11月3日