GSK-3536819
GSK plc의 5-in-1 1세대 백신 후보물질 GSK-3536819는 전 세계적으로 침습성 수막구균성 질환(IMD)을 가장 자주 유발하는 N.매닝티디스 박테리아 수막구균 다섯 그룹(A, B, C, W, Y;MenABCWY)을 표적으로 합니다. 이 백신은 이미 허가받은 GSK의 수막구균 백신인 BEXSERO(수막구균 그룹 B[MenB])와 MENVEO(MenACWY)의 항원 성분을 결합한 제품으로, 효능과 안전성 프로필이 입증되었습니다.

GSK-3536819 개요
- GSK plc
- 재조합 단백질, 외막 소포(OMV), N.메닝티디스 박테리아 수막구균 다섯 그룹(A, B, C, W, Y)을 표적으로 하는 접합성 5가 백신
- 10-25세 연령대가 적극적으로 예방 접종을 하도록 6개월 간격으로 2회 근육 주사 투여
- 2024년 미국 및 EU4(프랑스, 이탈리아, 스페인, 영국)시장에서 MenABCWY백신 접종 대상자수 6,400만
- 2024년 G7 시장에서 침습성 수막구균성 질환(IMD) 신규 증례 수 ~600
블록버스터 신약 선정 이유
MenB 백신과 MenACWY 백신을 결합하면 예방 효과는 유지하면서도 주사 횟수를 줄여 접종 범위와 일정 순응도를 개선할 수 있습니다.
GSK-3536819는 Pfizer의 5가 PENBRAYA™ 백신에 이어 두 번째로 출시되었으나, BEXSERO는 생후 2개월부터 접종이 가능해 유럽연합(EU)에서 승인을 받았다는 점에서 PENBRAYA의 Trumenba®(10세 이상 접종 가능) 대비 우위를 점하고 있습니다. 이로 인해 GSK-3536819는 EU에서 접종 가능한 인구 범위가 확대될 가능성이 있습니다. 이러한 다가 백신은 2030년까지 수막염 퇴치를 목표로 하는 WHO의 전략에도 기여할 수 있습니다.
GSK-3536819는 다섯 혈청군 모두에서 비열등성을 보였으며, 면역 반응 유도와 안전성 측면에서 BEXSERO 및 MENVEO와 유사한 프로필을 확인했습니다.
-
10~25세 건강한 성인 3,650명을 대상으로 두 차례(1일차 및 181일차) 백신을 투여한 중요한 글로벌 3상 임상시험입니다. 이는 BEXSERO의 확인 시험이기도 했습니다. 이 시험에서 백신은 110가지 B형 뇌수막염 침습성 균주에 대해 효과가 있었습니다.
-
이전에 MENVEO 백신을 접종한 적이 있는 15~25세 건강한 성인 1,247명을 대상으로 한 3B상 임상시험(1일차 및 181일차)에서 211일차에 GSK-3536819를 투여했습니다. 1일차에 MENVEO를 1회 투여하고 181일차와 211일차에 BEXSERO를 2회 투여하여 활성 비교군으로 삼았습니다.
심사 및 승인 현황
2024년 4월
BLA 승인: 미국 FDA
2025년 2월 14일
PDUFA 날짜
실제 및 예상 출시:
- 2024년: 미국
- 2025년: E.U., 영국
약물 일정 및 성공 확률
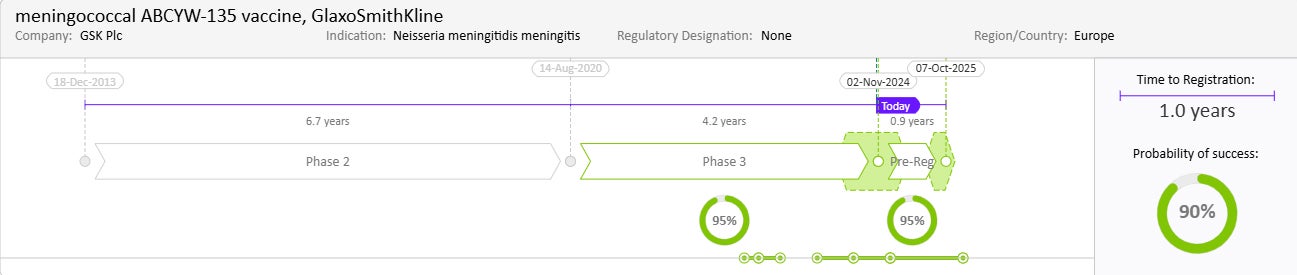
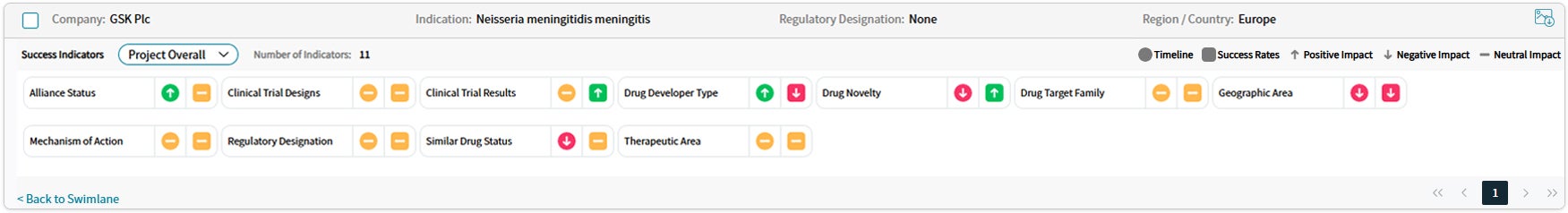
출처: Cortellis Competitive Intelligence, Drug Timeline & Success Rates Prediction, 2024년 10월 31일 기준
GSK-3536819가 수막구균 예방 시장에 미칠 영향은?
-
GSK-3536819는 같은 다섯 가지 혈청군(A, B, C, W, Y)에 대해 승인된 최초이자 유일한 5가 백신 PENBRAYA (Pfizer Inc)와 기존의 MenACWY 백신인 MENVEO, MenQuadfi®(Sanofi), NIMENRIX® (Pfizer Inc)와 경쟁할 것으로 예상됩니다.
-
PENBRAYA와 GSK-3536819 모두 투약 일정이 간단하여 의사들로부터 긍정적인 평가를 받고 있으며, 두 제품 모두 시장에서 성공적으로 자리 잡을 가능성이 높습니다.
-
5가 백신이 널리 보급됨에 따라 두 회사의 기존 ACWY 및 B 백신에 대한 수요는 감소할 가능성이 있습니다.
-
BEXSERO(50여 개국 판매)와 MENVEO(60여 개국 판매)의 2023년 매출은 각각 14% 증가한 8억 4,900만 파운드와 12% 증가한 3억 8,000만 파운드였습니다. GSK-3536819가 출시되면 일부 매출과 성장세가 GSK-3536819로 이동할 가능성도 있습니다.
GSK-3536819는 어떤 치료 공백을 메울 수 있는가?
침습성 수막구균성 질환(IMD)은 드물지만, 특히 어린이와 청소년에게 뇌 손상, 절단, 치명적 합병증 또는 사망과 같은 심각한 장기적 결과를 초래할 수 있는 질병입니다.GSK-3536819는 Pfizer의 PENBRAYA와 마찬가지로 전 세계적으로 발생하는 IMD 사례의 거의 대부분을 차지하는 다섯 가지 주요 혈청군(A, B, C, W, Y)을 예방할 수 있는 백신입니다.이 백신은 기존 방식처럼 두 가지 별도 백신을 맞을 필요 없이 단일 백신으로 두 번만 접종하면 됩니다. 이로 인해 백신 접종 순응도가 높아지고 취약 계층의 접종률을 증가시킬 수 있습니다.
블록버스터 신약이 되기 위해 극복해야 하는 문제는?
질병에 대한 인식 부족은 백신 접종률 저하로 이어질 수 있습니다. 예를 들어, 미국 청소년의 약 31%만이 수막구균 B 백신을 접종했으며, 필수 접종을 모두 완료한 비율은 12% 미만입니다.4
PENBRAYA는 미국 시장에서 10~25세 연령대를 대상으로 승인되어 2023년 9월 기준으로 1년 이상 판매된 첫 5가(A, B, C, W, Y) 수막구균 백신으로, 시장 선점의 이점을 가지고 있습니다.
GSK-3536819가 전 세계적으로 승인되더라도 일부 지역에서는 도입이 지연될 가능성이 있습니다. 이는 특히 여건이 열악한 국가와 지역에서 특정 유행 균주를 예방하는 단가 백신에 비해 비용이 높기 때문입니다.