Talquetamab 소개
-
제조사:Johnson & Johnson Innovative Medicine
-
CD3 및 GPRC5D를 표적으로 하는 이중 특이항체
-
R/R 다발성 골수종 치료를 위해 주1회 또는 격주 1회 피하 투여
-
~10만 5천건: 2023년 G7 시장에서 재발성 또는 불응성 다발성 골수종 진단 증례

Talquetamab은 다발성 골수종 치료를 위한 계열 내 최초 CD3 및 GPRC5D 표적 이중 특이항체로, EC와 FDA로부터 각각 조건부 및 신속 승인을 받았습니다.
재발성 또는 불응성(relapsed or refractory, R/R) 다발성 골수종 환자를 대상으로 한 중추적인 제1/2상MonumenTAL-1시험을 기반으로 연구 및 승인이 이루어졌습니다. 현재 진행 중인 제3상 임상시험을 통해 Talquetamab의 승인된 환경에서 임상적 유익성을 확인하고 다른 다발성 골수종 환자 집단에서 승인된 다른 약제와의 병용(예: DARZALEX®, Johnson & Johnson Innovative Medicine)을 포함한 적응증 확대로 이어질 것으로 예상됩니다. Talquetamab은 자주 재발하는 난치성 질환인 다발성 골수종 치료제에 추가적으로 중요한 역할을 할 것으로 기대됩니다.

Talquetamab의 승인으로 Johnson & Johnson Innovative Medicine은 다발성 골수종 환자의 미충족요구를 해결하기 위한 포트폴리오에 두 가지 이중 특이항체를 포함한 5개의 혁신 요법을 추가하게 되었습니다. Talquetamab은 다발성 골수종 치료를 위해 연구되고 있는 CD3 및 GPRC5D를 표적으로 하는 기성의 계열 내 최초, T세포 결합 이중 특이 항체입니다. 프로테아좀 억제제, 면역조절제, 항-CD38 단일클론항체 등 이전에 4차 이상의 요법을 투여받은 적이 있는 환자를 대상으로 실시한 중추적 제1/2상 임상시험 MonumenTAL-1에서 긍정적인 결과가 보고되었습니다. 환자의 1/3도 임상시험 참가 이전에 BCMA표적 치료를 받았습니다. 시험결과는 다음과 같습니다:
MonumenTAL-3의 임상 3상은 현재 진행중입니다. 본 임상은 적어도 하나의 이상의 이전 치료를 받은 R/R다발성 골수종 환자를 대상으로 하며 Talquetamab와 Daratumumab 병용 치료를 Daratumumab,Pomalidomide 및 Dexamethasone 병용치료와 비교하여 진행됩니다.
2021년 1월
2021년 5월
2021년 8월
2022년 6월
2023년 9월
2023년8월
프로테아좀 억제제, 면역조절제, 항-CD38 mAb를 포함하여 4차 이상의 이전 요법을 투여받았던 재발성 또는 불응성 다발성 골수종 환자 대상
이전에 면역조절제, 프로테아좀 억제제, 항-CD38 mAb를 포함한 3차 이상의 이전 요법을 투여받은 적이 있고 마지막 요법에서 질병 진행이 입증된 재발성 또는 불응성 다발성 골수종 환자 대상
실제 및 예상 출시:
특허 만료시기: 2037년 이후
Talquetamab이 다발성 골수종 치료제 시장에 미칠 영향은?
다발성 골수종은 고가의 소분자 및 생물학적 제제로 구성된 병용 요법이 치료의 주류를 이루고 있기 때문에 종양학 분야에서 가장 큰 치료시장입니다. 높은 치료율, R/R 질환에 대한 많은 잠재적 치료법, 일부 요법의 긴 치료 기간이 이 시장의 규모를 견인하고 있습니다
Talquetamab은 어떤 치료 공백을 메울 수 있는가?
다발성 골수종 환자의 재발율이 높기 때문에 후속 요법이 필요합니다. 또한 새로운 차수의 요법을 사용하면 질병 진행에 따라 관해 기간이 짧아집니다. Talquetamab이 모든 치료 옵션은 아니더라도 대부분의 치료 옵션이 소진된 치료가 어려운 다발성 골수종 환자의 치료에 대해 승인되어 보다 효과적인 치료법에 대한 미충족된 요구를 해소하는데 도움이 될 것입니다. 또한 이는 기성품(off-the-shelf product)이기 때문에 환자 맞춤형 CAR-T세포 요법에 비해 이점이 있으며, 항BCMA 요법에서 질병이 진행된 환자에게도 치료 옵션을 제공합니다.
Talquetamab이 블록버스터 신약이 되기 위해 극복해야 하는 문제는?
생명을 위협하거나 치명적인 사이토카인 방출 증후군(cytokine release syndrome, CRS) 및 면역 효과기 세포 관련 신경독성(immune effector cell-associated neurotoxicity, ICANS)을 포함한 신경독성에 대한 블랙박스 경고 라벨로 인해 투여가 저해될 수 있습니다. 따라서 Talquetamab은 처방의가 인증을 받아야 하는 TECVAYLI 및 TALVEY 위해성 평가 및 완화 전략(Risk Evaluation and Mitigation Strategy, REMS)을 통해서만 사용할 수 있습니다. 또한 다른 이중 특이요법과 치열한 경쟁에 직면할 수 있습니다.
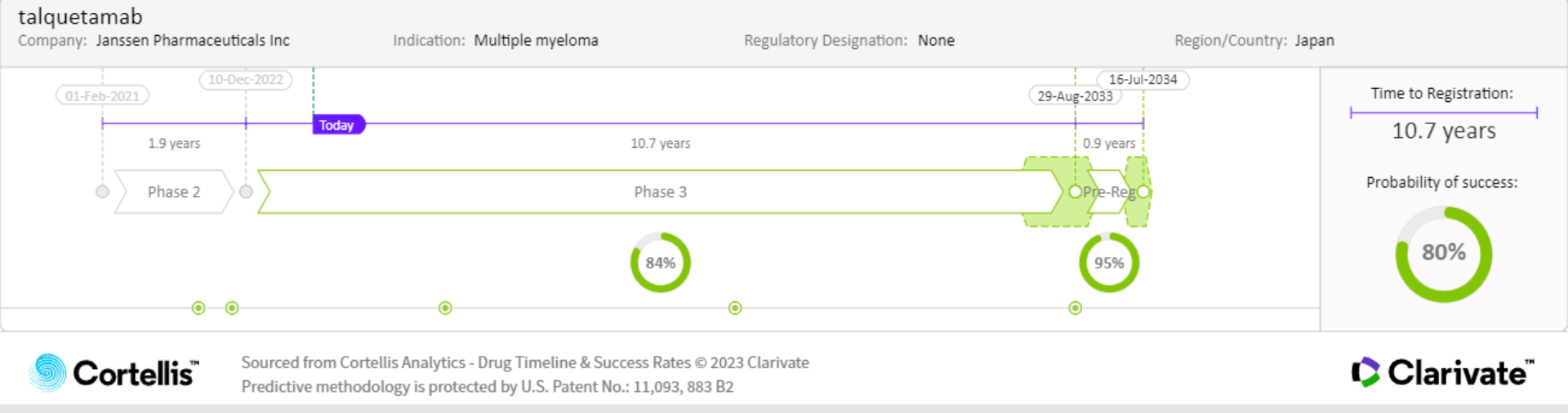
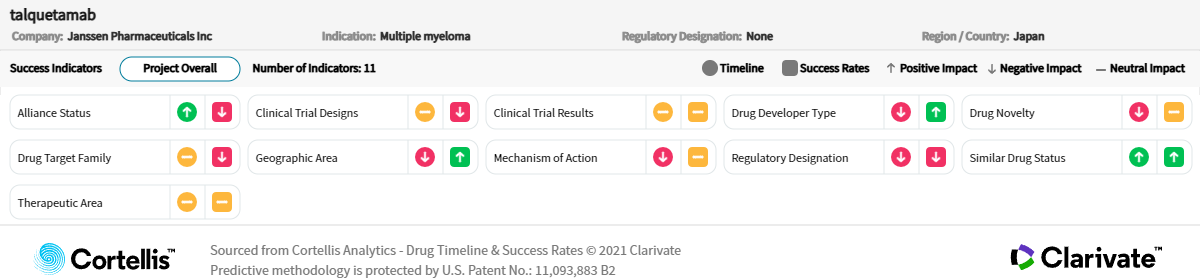
출처: Cortellis Competitive Intelligence, Drug Timeline & Success Rates Prediction, 2023년 11월 3일 기준