斑塊型乾癬
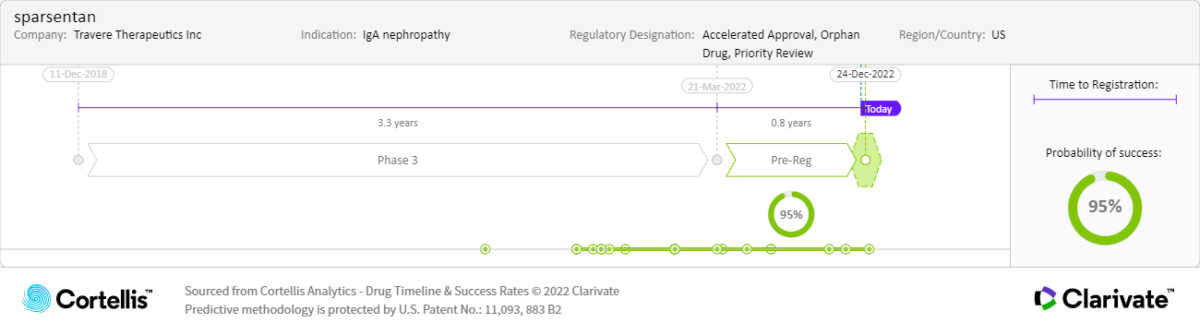
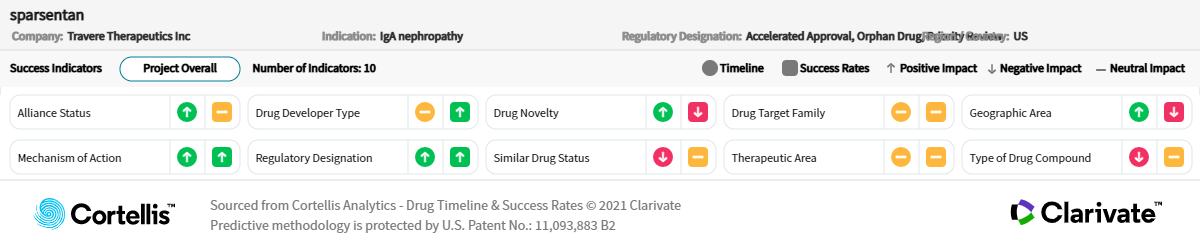
關於Sparsentan
-
生產商:Travere Therapeutics Inc
-
雙重內皮素血管收縮素受體拮抗劑(DEARA)
-
每日口服給藥,治療 IgA 腎病和FSGS
-
IgA 腎病:全球約有20 萬- 35 萬 IgA 腎病患者
-
FSGS:患病率為七百萬分之一

Sparsentan 是一種口服單分子 first-in-class 新藥,可作為內皮素 A(ETA)受體和血管收縮素 II 亞型 1(AT1)受體的高親和力雙效拮抗劑,這兩種受體都與腎臟疾病的進展相關。該藥物的開發針對 IgA 腎病和 FSGS,其有望阻止許多患者的病情進展,並填補治療手段的空白。